

 Ru | En
Ru | En



 Ru | En
Ru | En

 …В свое время открытие антибиотиков произвело настоящую революцию в медицине, однако уже сейчас, по прошествии времени, ученые и эксперты в области здравоохранения вынуждены признать, что возбудители инфекционных заболеваний научились приспосабливаться к действию этого типа лекарственных средств. Одно из решений проблемы — разработка препаратов принципиально нового поколения. Об альтернативе традиционным антибиотикам, создаваемой на основе антимикробных пептидов, бактерий — симбионтов энтерококков — интервью «НУ» с научным сотрудником Института клеточного и внутриклеточного симбиоза УрО
…В свое время открытие антибиотиков произвело настоящую революцию в медицине, однако уже сейчас, по прошествии времени, ученые и эксперты в области здравоохранения вынуждены признать, что возбудители инфекционных заболеваний научились приспосабливаться к действию этого типа лекарственных средств. Одно из решений проблемы — разработка препаратов принципиально нового поколения. Об альтернативе традиционным антибиотикам, создаваемой на основе антимикробных пептидов, бактерий — симбионтов энтерококков — интервью «НУ» с научным сотрудником Института клеточного и внутриклеточного симбиоза УрО  РАН (г. Оренбург), лауреатом стипендии президента РФ для молодых ученых, кандидатом биологических наук Алексеем Васильченко.
РАН (г. Оренбург), лауреатом стипендии президента РФ для молодых ученых, кандидатом биологических наук Алексеем Васильченко.
— Алексей Сергеевич, в чем преимущество антимикробных пептидов по сравнению с классическими антибиотиками?
— Не секрет, что одна из самых серьезных проблем современной санитарной и клинической медицины — устойчивость микроорганизмов к используемым в клинической практике антибиотикам. Помощник генерального директора ВОЗ по вопросам безопасности в области здравоохранения доктор Кейджи Фукуда даже назвал антибиотикорезистентность одним из основных глобальных вызовов, с которой столкнулось человечество в настоящее время. Сложность состоит в том, что в мире микроорганизмов все процессы изменчивости и отбора происходят чаще и проявляются быстрее, а значит, вновь созданный препарат для борьбы с инфекцией необязательно будет абсолютной панацеей.
Вместе с тем антимикробные пептиды в определенном смысле также являются антибиотиками, но иного происхождения. Это синтезируемые на рибосомах короткие последовательности аминокислот, которые в силу своих физико-химических свойств эффективно воздействуют на микроорганизмы, подавляя их развитие. Поскольку способностью синтезировать такие пептиды обладают многие живые существа, она рассматривается как наиболее древний и универсальный механизм защиты организма от чужеродных агентов.
Антибиотикорезистентность обусловлена различными факторами: микроорганизмы научились либо изменять ту мишень, на которую направлено действие антибиотика, либо разрушать антибиотик «на подлете», производя соответствующие ферменты. В то же время большинство антимикробных пептидов воздействуют в основном на клеточную стенку бактерий. Поскольку это та структура, которая делает клетку клеткой, изменить ее основные характеристики и выработать устойчивость микроорганизму не так-то просто. Кроме того, подобные преобразования чрезвычайно нагружают метаболизм бактерии. Поэтому резистентность к антимикробным пептидам если и возникает, то в редких случаях и зачастую является временной. В этом и заключается преимущество подобных веществ перед традиционными антибиотиками.
— И как в этом деле могут помочь энтерококки?
—Энтерококки — это микроорганизмы, которые наряду с лакто- и бифидобактериями обитают в кишечнике человека и животных, принимая участие в формировании естественного иммунитета организма-хозяина. Несмотря на это они также могут быть причиной различных инфекций, в том числе с серьезными последствиями для носителя. Двойственная роль этих бактерий в симбиозе с макроорганизмом и есть причина, по которой энтерококки — предмет пристального изучения ученых различных стран. И здесь интерес в первую очередь связан с антагонистической активностью этих бактерий по отношению к ряду болезнетворных микробов.
— То есть сами энтерококки вырабатывают антимикробные пептиды?
— Да, они, как и другие бактерии, продуцируют такого рода пептиды. Их также называют бактериоцинами или, в случае с энтерококками, энтероцинами. Бактериоцины позволяют продуцирующим их бактериям регулировать численность внутри популяции, а также воздействовать на представителей близких видов. Сама выработка пептидов происходит в ответ на внешнее воздействие. Дело в том, что популяция микроорганизмов — это не просто скопление клеток, а некая социальная структура со своим способом общения между ее представителями, с так называемым «чувством кворума». А реализуется это общение за счет различных химических веществ — аутоиндукторов чувства кворума, которые вырабатываются всеми членами популяции. Стоит только популяции разрастись до критических значений, как запускаются механизмы регуляции. Именно в ответ на воздействие аутоиндукторов и вырабатываются, в частности, бактериоцины.
— Чем пептиды, полученные от энтерококков, отличаются от пептидов, полученных от другого рода бактерий?
— Существует универсальная классификация бактериоцинов. Она включает четыре группы, различающиеся структурой, физико-химическими свойствами, особенностями синтеза и секреции. Энтерококки продуцируют бактериоцины, относящиеся к трем наиболее представительным группам и очень похожие на бактериоцины, производимые другими молочнокислыми бактериями. Возможно, более интересным был бы вопрос, чем отличаются антимикробные пептиды бактерий от продуцируемых другими организмами? И здесь исследователи выделяют несколько основных отличий. Во-первых, антимикробное действие бактериоцинов распространяется на относительно узкий круг микроорганизмов, и при создании препаратов такая избирательность может иметь значение. Во-вторых, действующие концентрации бактериоцинов зачастую на порядок меньше по сравнению с антимикробными пептидами, например, животного происхождения. И, в-третьих, бактериционы не оказывают повреждающего действия на клетки организма.
— В отношении каких инфекций они могут быть эффективны?
— Круг чувствительных микроорганизмов включает такие патогены, как листерии, стафилококки, бациллы, вызывающие инфекции человека и животных.
— Какой путь нужно пройти, чтобы перейти к созданию лекарственных средств на основе антимикробных пептидов энтерококков?
— Среди пептидных антибиотиков, уже используемых в практической жизни человека, наиболее известен препарат на основе низина — бактериоцина, производимого лактобактериями. Это средство одобрено управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и эффективно подавляет листерии, опасных возбудителей пищевых инфекций. Поэтому в первую очередь оно используется как пищевой консервант. Другая форма применения — это пробиотики, т.е. вещества, используемые уже в терапевтических целях. Так вот, хотя пробиотики, созданные на основе культур бактериоциногенных микроорганизмов, и позволяют добиться хороших результатов в профилактике пищевых инфекций, непосредственно целей терапии они малоэффективны. Более перспективным представляется введение в организм так называемого очищенного бактериоцина, и здесь необходимо преодолеть ряд трудностей.
Во-первых, микроорганизмы в естественных условиях секретируют очень незначительное количество антимикробных пептидов, и поэтому необходимы какие-то манипуляции по увеличению их выработки. Во-вторых, лабораторные методы очистки целевого вещества от примесей позволяют получить в лучшем случае миллиграммовые количества. В-третьих, предстоит найти оптимальный способ доставки препарата на основе бактериоцинов к месту инфекционного процесса.
Но прежде чем перейти к созданию препарата в промышленных масштабах, необходимо провести лабораторные исследования: изучить структурные характеристики вещества, биологические особенности продукции и антимикробного действия, включая исследования токсических свойств в отношении животного организма. В частности, наша лаборатория дисбиозов имеет многолетний опыт исследования энтерококков, выделенных из кишечника человека. При этом к настоящему моменту создана коллекция микроорганизмов, включающая несколько сотен уникальных штаммов энтерококков, значительная часть которых демонстрирует способность подавлять возбудителей инфекций. Последние работы сконцентрированы именно на получении чистых препаратов бактериоцинов и изучении их физико-химических характеристик, а также исследовании механизмов антимикробного действия на клеточном и молекулярном уровне. Но путь к созданию лекарственного средства долог, труден и дорог. Статистика такова, что множество различных антимикробных пептидов уже прошли ряд доклинических испытаний, но препаратов, прреодолевших все необходимые этапы, пока еще очень мало.
Подготовил Павел КИЕВ
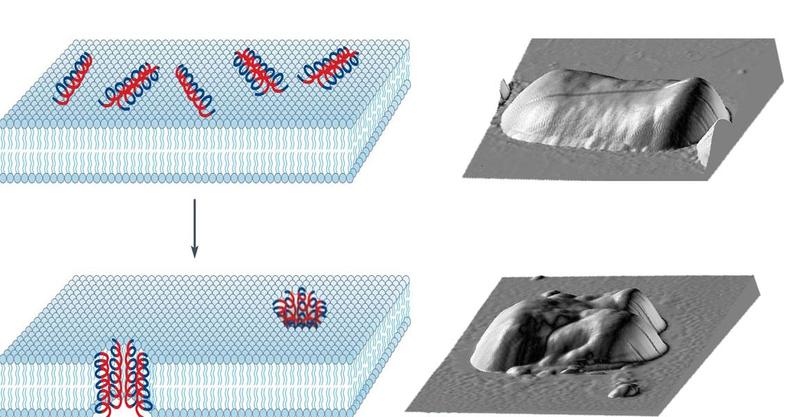
В центре — схема действия бактериоцина;
слева — А.С. Васильченко.
|
620049, г. Екатеринбург, ул. Первомайская, 91 +7(343) 374-07-47 |