

 Ru | En
Ru | En



 Ru | En
Ru | En

 В 2014 году коллектив российских ученых, который возглавлял тогда член-корреспондент РАН Владимир Семенович Мархасин, получил грант Российского научного фонда на разработку персонифицированных математических моделей в кардиологии. Благодаря современным средствам компьютерной диагностики человек сегодня может быть просканирован от головы до пят, и все же врач не всегда может поставить правильный диагноз, а тем более предсказать сценарий развития заболевания у конкретного пациента. Создание персонифицированных, ориентированных на пациента интегративных математических и компьютерных моделей особенно актуально в случае сердечно-сосудистой патологии в силу исключительной сложности структуры и функций сердца и многочисленности параметров, определяющих эти функции.
В 2014 году коллектив российских ученых, который возглавлял тогда член-корреспондент РАН Владимир Семенович Мархасин, получил грант Российского научного фонда на разработку персонифицированных математических моделей в кардиологии. Благодаря современным средствам компьютерной диагностики человек сегодня может быть просканирован от головы до пят, и все же врач не всегда может поставить правильный диагноз, а тем более предсказать сценарий развития заболевания у конкретного пациента. Создание персонифицированных, ориентированных на пациента интегративных математических и компьютерных моделей особенно актуально в случае сердечно-сосудистой патологии в силу исключительной сложности структуры и функций сердца и многочисленности параметров, определяющих эти функции.
Для исполнения проекта в Уральском федеральном университете была создана лаборатория математического моделирования в физиологии и медицине с использованием суперкомпьютерных технологий. Участниками проекта стали также сотрудники Института иммунологии и физиологии и Института математики и механики Уральского отделения РАН, Научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева и Свердловской областной клинической больницы №1, Института механики МГУ и Гентского университета (Бельгия). В этом мультидисциплинарном исследовании заняты специалисты в области физиологии и медицины, биофизики и биомеханики, математики и компьютерных наук.
Трудности моделирования
О ходе выполнения проекта и его конечных целях мы поговорили с руководителем гранта доктором физико-математических наук Ольгой Соловьевой, которая возглавляет инновационную лабораторию УрФУ.
— Моделированием сердечной мышцы активно занимаются ученые разных стран. В чем уникальность вашего проекта?
— Подобные проекты реализуются и в нашей стране, и в США, Великобритании, Новой Зеландии, Японии, Китае. Причем наибольшие успехи достигнуты в построении электрофизиологических моделей сердца в норме и при патологии, которые широко внедряются в клиническую практику. Например, на основе компьютерных моделей в НЦ сердечнососудистой хирургии им. А.Н. Бакулева создан аппаратно-программный комплекс «АМИКАРД» для определения источников нарушения сердечного ритма и их купирования.  Гораздо менее разработаны модели механической функции сердца, а тем более модели, в которых интегрируются электрические и механические процессы на клеточном и тканевом уровне и учитываются прямые и обратные связи между ними. И еще один важнейший момент. Дело в том, что миокард — это анизотропная среда, где электрический сигнал распространяется в разных направлениях неодинаково, с разной скоростью, и зависит это от хода волокон сердечной мышцы. Активный механический сигнал также формируется и действует вдоль этих волокон. Поэтому для построения реалистичной модели мало знать геометрию камер сердца, важно представлять, как расположены волокна в их стенках.
Гораздо менее разработаны модели механической функции сердца, а тем более модели, в которых интегрируются электрические и механические процессы на клеточном и тканевом уровне и учитываются прямые и обратные связи между ними. И еще один важнейший момент. Дело в том, что миокард — это анизотропная среда, где электрический сигнал распространяется в разных направлениях неодинаково, с разной скоростью, и зависит это от хода волокон сердечной мышцы. Активный механический сигнал также формируется и действует вдоль этих волокон. Поэтому для построения реалистичной модели мало знать геометрию камер сердца, важно представлять, как расположены волокна в их стенках.
В свое время, в частности, в рамках проекта «Виртуальное сердце», мы разработали базовые модели электрической и механической функции сердечной клетки, ткани, тонкой архитектоники стенок левого желудочка. Это так называемые «популяционные», идеализированные модели, которые описывают некоторое усредненное для популяции (животных или человека) поведение сердца как органа. Но эта модель как бы «безликая». В рамках нынешнего проекта перед нами стоит задача адаптировать популяционную модель к конкретному пациенту с учетом индивидуальных параметров его сердечно-сосудистой системы и особенностей течения его заболевания.
— И на выходе предполагается получить…
— …интегративную трехмерную модель левого желудочка, сопряженную с упрощенной моделью сосудистой системы. Далее эта модель персонифицируется на основе данных о функциональной геометрии, электрофизиологии и механике левого желудочка конкретного пациента и подвергается специальным тестовым испытаниям, которые позволят объективно оценить функциональные возможности левого желудочка и получить прогноз нарушений его механической и электрической функции.
Все начинается в клинике 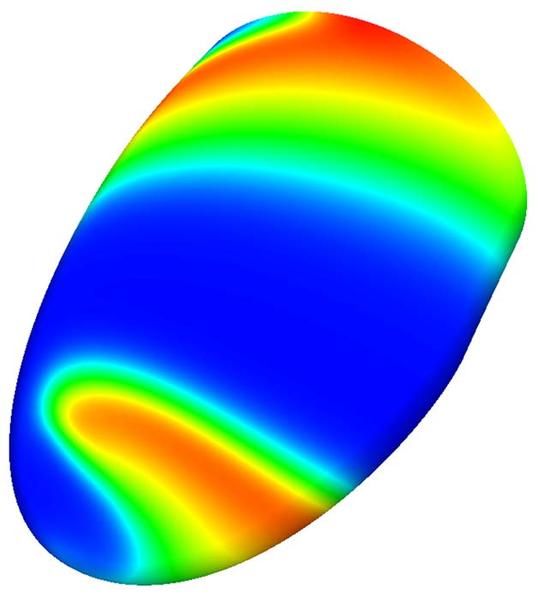 Данные для построения математических моделей ученым предоставляют сотрудники Областной клинической больницы №1 (Екатеринбург), Научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева (Москва) и других медицинских учреждений. Кардиологи и кардиохирурги проводят отбор больных с различными аномалиями геометрии и функции сердца. Есть и референтная группа «нормальных сердец». Изображения миокарда получают методами магниторезонансной томографии (МРТ), компьютерной томографии (КТ) и эхокардиографии (УЗИ). У пациентов и здоровых людей определяют основные показатели геометрии левого желудочка в течение сократительного цикла: линейные размеры, толщину стенки, индексы формы (сферичность, коничность, индекс Фурье) и другие. Современные методы исследования сердечно-сосудистой системы позволяют получить информацию о молекулярных механизмах возникновения болезни и структурных изменениях сердца и сосудов у больных с аритмиями и сердечной недостаточностью, клапанными и сосудистыми заболеваниями. Все эти показатели затем используются в качестве входных параметров 3D модели.
Данные для построения математических моделей ученым предоставляют сотрудники Областной клинической больницы №1 (Екатеринбург), Научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева (Москва) и других медицинских учреждений. Кардиологи и кардиохирурги проводят отбор больных с различными аномалиями геометрии и функции сердца. Есть и референтная группа «нормальных сердец». Изображения миокарда получают методами магниторезонансной томографии (МРТ), компьютерной томографии (КТ) и эхокардиографии (УЗИ). У пациентов и здоровых людей определяют основные показатели геометрии левого желудочка в течение сократительного цикла: линейные размеры, толщину стенки, индексы формы (сферичность, коничность, индекс Фурье) и другие. Современные методы исследования сердечно-сосудистой системы позволяют получить информацию о молекулярных механизмах возникновения болезни и структурных изменениях сердца и сосудов у больных с аритмиями и сердечной недостаточностью, клапанными и сосудистыми заболеваниями. Все эти показатели затем используются в качестве входных параметров 3D модели.
Компьютерной обработкой изображений сердца и построением на их основе трехмерной математической модели миокарда занимаются специалисты Института математики и механики УрО РАН — сотрудники отдела вычислительной техники, которым заведует кандидат технических наук Андрей Созыкин, и сектора математического моделирования в кардиологии во главе с кандидатом физико-математических наук Сергеем Правдиным. Картинки с УЗИ, полученные в клинике, не всегда четкие, и их обработка — дело трудоемкое. Но это только первый этап. Компьютерная модель сердца — это сетки, состоящие из сотен тысяч элементов, и работа с ними требует больших вычислительных мощностей. В ИММ УрО РАН это делается на суперкомпьютере «УРАН».
По словам Сергея Правдина, самое трудное — создать такую модель левого желудочка миокарда человека, чтобы ее можно было достаточно легко «подогнать» к сердцу конкретного пациента.
— Наша группа специализируется на моделировании электрической функции миокарда, — говорит Правдин. — В частности, в рамках проекта мы под руководством профессора Александра Панфилова изучаем на уровне клетки, ткани и органа динамику трехмерных вихрей электрического возбуждения в миокарде, возникающих при аритмии. Благодаря компьютерному моделированию врач может видеть на экране монитора, как эти вихри формируются и распадаются и какие факторы этому способствуют.
…и в клинику возвращается  О том, насколько необходима сегодня доктору виртуальная модель, интегрирующая лабораторно-клинические данные об изменении структуры и функции сердечно-сосудистой системы больного, нам рассказал зав. отделением хирургического лечения нарушений ритма сердца и электрокардиостимуляции Свердловской областной клинической больницы № 1, заслуженный врач РФ, кандидат медицинских наук Сергей Михайлов, также участник проекта (на фото вверху):
О том, насколько необходима сегодня доктору виртуальная модель, интегрирующая лабораторно-клинические данные об изменении структуры и функции сердечно-сосудистой системы больного, нам рассказал зав. отделением хирургического лечения нарушений ритма сердца и электрокардиостимуляции Свердловской областной клинической больницы № 1, заслуженный врач РФ, кандидат медицинских наук Сергей Михайлов, также участник проекта (на фото вверху):
— Мостик между учеными-кардиофизиологами и нами, клиницистами, сформировался благодаря союзу, к сожалению, уже ушедших из жизни Владимира Семеновича Мархасина и руководителя кардиохирургической клиники ОКБ №1 Милослава Станиславовича Савичевского. Для нас главное — изучение механизмов сердечной недостаточности. Неважно, чем она вызвана — пороками сердца, артериальной гипертензией, миокардитом или инфарктом миокарда, результат всегда один — снижение насосной функции сердца. Это может быть связано с нарушением проведения электрического сигнала в камерах сердца, например, один желудочек сокращается, а другой еще нет, или задержка происходит при проведении сигнала от предсердия к желудочку. Чтобы добиться улучшения насосной функции, мы применяем ресинхронизирующую терапию, или, проще говоря, имплантируем трехкамерные электрокардиостимуляторы. Очень важно разместить их электроды правильно, а «вслепую» сделать это трудно. Вот почему так нужна виртуальная модель — на ней мы можем проигрывать разные сценарии развития сердечной недостаточности, изучать резерв насосной функции сердца пациента, отрабатывать технологии установки кардиостимуляторов, оценивать эффект лечения и возможные риски.
В персонифицированной модели сердечно-сосудистой системы на молекулярно-клеточном уровне можно также исследовать действие лекарственных препаратов, а например, в случае инфаркта миокарда модель будет способна предсказать оптимальные варианты хирургического вмешательства.
Общеизвестно, что сегодня сердечно-сосудистая патология занимает первое место среди причин смертности, а хронической сердечной недостаточностью страдают десятки миллионов людей. Радует, что российские ученые и клиницисты успешно работают на преодоление этой печальной статистики.
Е. ПОНИЗОВКИНА
|
620049, г. Екатеринбург, ул. Первомайская, 91 +7(343) 374-07-47 |