

 Ru | En
Ru | En



 Ru | En
Ru | En

 Газовые гидраты — необычные соединения, похожие на снег, — уже давно исследуют в лаборатории фазовых переходов и неравновесных процессов Института теплофизики УрО РАН. Уральские ученые предложили собственный способ получения газовых гидратов и сейчас ведут эксперименты. Подробнее об этой работе и перспективах, которые гидраты могут открыть для водородной энергетики, корреспонденту «НУ» рассказал старший научный сотрудник лаборатории, кандидат физико-математических наук Андрей Владимирович Виноградов.
Газовые гидраты — необычные соединения, похожие на снег, — уже давно исследуют в лаборатории фазовых переходов и неравновесных процессов Института теплофизики УрО РАН. Уральские ученые предложили собственный способ получения газовых гидратов и сейчас ведут эксперименты. Подробнее об этой работе и перспективах, которые гидраты могут открыть для водородной энергетики, корреспонденту «НУ» рассказал старший научный сотрудник лаборатории, кандидат физико-математических наук Андрей Владимирович Виноградов.
— Газовые гидраты — твердые кристаллические вещества, особые соединения с водой. Эти соединения образуются, когда молекула «вещества-гостя», например газа, помещена в полость внутри кристаллической решетки, состоящей из молекул воды — «вещества-хозяина».
И это не какие-то фантастические соединения, придуманные учеными. Газовые гидраты широко встречаются в природе. Существенные запасы углеводородного сырья, в основном метана, находятся именно в газогидратном виде. Более того, эти запасы заметно превышают запасы топлива на Земле во всех остальных видах, вместе взятых. Основная масса гидратов залегает на дне океанов, под толщей воды и, соответственно, под большим давлением. По этой причине эти запасы не могут добываться привычным для нас бурением.
Есть также основания предполагать, что газовые гидраты широко распространены и в других уголках Вселенной. Имеющиеся данные свидетельствуют о наличии условий для образования и существования гидратов на всех планетах Солнечной системы, за исключением Меркурия и Венеры, а также на некоторых спутниках и астероидах.
По внешнему же виду гидрат напоминает снег или рыхлый лед. Его можно даже взять в руки, и если он начнет таять, из него выделится колоссальное количество газа.— О каких объемах идет речь?
— При таянии одного литра этого «снега» выделится около 160 литров газа. Между тем для того, чтобы поместить в баллон сходный объем газа в его обычном состоянии, понадобится подать очень сильное давление — 160 атмосфер. В случае же с гидратами потребность в сверхвысоких давлениях отпадает, поэтому интерес к таким веществам для целей хранения и транспортировки газов огромен. Но есть одна тонкость — температура должна быть не выше 0°C.
Интересно, что гидраты при атмосферном давлении разлагаются на воду и газ при довольно низких температурах, например, для гидрата метана такая температура составляет –80о С. Но в состоянии неустойчивого равновесия или в так называемом метастабильном состоянии гидраты некоторых газов могут существовать вплоть до температуры таяния льда — 0о С. Эта способность объясняется эффектом самоконсервации, когда с поверхности гидрата при его разложении уходит газ и объем покрывается, как скорлупой, коркой льда, которая мешает дальнейшему разложению гидрата. Примечательно, что консервация происходит сама собой, для этого не нужно ничего делать — природа сама все устроила.
— Как возник интерес к газовым гидратам? — В нашем институте еще в 1970-е годы занимались исследованием низкотемпературных аморфных конденсатов воды и неорганических жидкостей. В 2010 году заведующий нашей лабораторией член-корреспондент Владимир Петрович Коверда предложил эксперимент, в ходе которого на поверхность, охлажденную до температуры жидкого азота, подавались бы в вакууме одновременно разреженный водяной пар и газ. И то, и другое, естественно, в результате быстро замерзает. Вода при такой температуре переходит в состояние насыщенного газом аморфного льда, твердого вещества, не имеющего, подобно стеклу, строго упорядоченной структуры. При последующем нагреве подвижность молекул воды возрастает, они начинают выстраиваться в кристаллическую решетку, захватывая молекулы газа. В результате образуются газовые гидраты.
— В нашем институте еще в 1970-е годы занимались исследованием низкотемпературных аморфных конденсатов воды и неорганических жидкостей. В 2010 году заведующий нашей лабораторией член-корреспондент Владимир Петрович Коверда предложил эксперимент, в ходе которого на поверхность, охлажденную до температуры жидкого азота, подавались бы в вакууме одновременно разреженный водяной пар и газ. И то, и другое, естественно, в результате быстро замерзает. Вода при такой температуре переходит в состояние насыщенного газом аморфного льда, твердого вещества, не имеющего, подобно стеклу, строго упорядоченной структуры. При последующем нагреве подвижность молекул воды возрастает, они начинают выстраиваться в кристаллическую решетку, захватывая молекулы газа. В результате образуются газовые гидраты.
В итоге эксперимент нами был проведен, и высказанные предположения подтвердились. Были получены образцы гидратов разных газов, в том числе компонентов природного газа. Подчеркну, что мы предложили новый способ гидратообразования, отличный от тех, которые используются исследователями в настоящее время.
Главное достижение состоит в том, что теперь мы можем легко получать образцы гидратов в лабораторных условиях и в последующем исследовать их свойства. Работа в этом направлении ведется.
— Насколько предложенный вами способ получения гидратов пригоден для оптимизации транспортировки природного газа?
— В лаборатории мы получаем гидраты в небольших количествах, но вполне возможно, что нашим способом их можно получать и в промышленных масштабах. Но для этого нужно рассчитать экономическую целесообразность такого производства.
Как сейчас организована транспортировка газа? Один из основных способов — доставка под высоким давлением по трубам. В них, кстати, из-за паров воды также образуются гидраты, но уже как вредное отложение. Через каждые 150 километров трубопровода стоят насосные станции, которые повышают давление в трубе, чтобы газ двигался вперед. Сооружение и обслуживание таких станций требует существенных затрат. А для перевозки газа в гидратном состоянии, по сути, нужен лишь «термос». Никаких проблем с поддержанием температурного режима при транспортировке быть не должно — возим же мы как-то замороженные овощи и фрукты. Тем более речь здесь не идет о крайне низких температурах, а лишь о –4°C.
Таким способом мы можем перемещать большое количество газа при его малом физическом объеме в гидратном состоянии, не создавая при этом никаких специальных условий, кроме температуры. Высокое давление — это же всегда опасность. Любой удар по емкости со сжатым газом может привести к взрыву.
Однако, как я уже говорил, перспективность гидратов для целей транспортировки природного газа еще нужно оценить с экономической точки зрения. Допускаю, что заключение может быть отрицательным. Но, например, у японцев есть установка по производству гидратов, рассчитанная на пять тонн в сутки. Они производят гидраты для транспортировки в какой-то отдаленный поселок, где «снег» плавят и получают газ. Японцы создали такую установку в середине 2000-х годов и посчитали для себя такой способ доставки газа экономически обоснованным.
Но цель нашей работы, которую мы сами себе ставим, заключается отнюдь не в получении гидратов компонентов природного газа, а в получении гидрата водорода. Решение этой проблемы, вероятно, будет иметь большую экономическую целесообразность.
— Почему именно водорода?
— Водород — интересный элемент. В чистом виде вы его никогда не сможете долго удержать. Если закачать водород в железный баллон, то молекулы H2 тут же отдадут свои свободные электроны, и от них останутся лишь ядра. А ядро водорода настолько маленькое, что оно легко проскальзывает через металл наружу.
Поэтому водород длительно хранят другими способами, как правило, в виде различных соединений. И здесь наша цель — получить клатратное соединение с водородом. С этим есть некоторые технические сложности. Для того чтобы получить первые образцы гидрата водорода, нам нужны температуры жидкого гелия, которые близки к абсолютному нулю. Использование жидкого гелия в массовом производстве будет очень дорогим и скорее всего экономически нецелесообразным, поэтому мы проводим работы в направлении повышения температуры, при которой можно получить гидрат водорода.
Немаловажный фактор для успешного проведения работы — это заинтересованный коллектив, который пополняется молодыми сотрудниками с новыми идеями. К счастью, недавно к нам пришел студент, он подготовил и защитил под моим руководством дипломную работу. Сейчас он собирается поступать к нам в аспирантуру. Включится в работу — эксперименты пойдут с большей интенсивностью.
— Где может найти применение водород?
— Движение в сторону водородной энергетики относится к числу приоритетных задач, поставленных государством в области развития науки, технологий и техники. И здесь существует множество проблем, одна из которых — вопрос хранения водорода. Предлагаются разные способы, но все они дорогие и сложные. Например, так называемые металлогидриды — соединения металла с водородом. При одних условиях он поглощает водород, при других — отдает. С гидратом водорода, по-моему, все будет гораздо проще. Это соединение существует, есть его описания. Мы лишь хотим получать его нашим способом.
Беседу вел Павел КИЕВ
На фото: заведующий лабораторией фазовых переходов и неравновесных процессов член-корреспондент В.П. Коверда, старший научный сотрудник А.В. Виноградов, заместитель директора ИТФ УрО РАН М.З. Файзуллин и стажер-исследователь А.С. Томин.
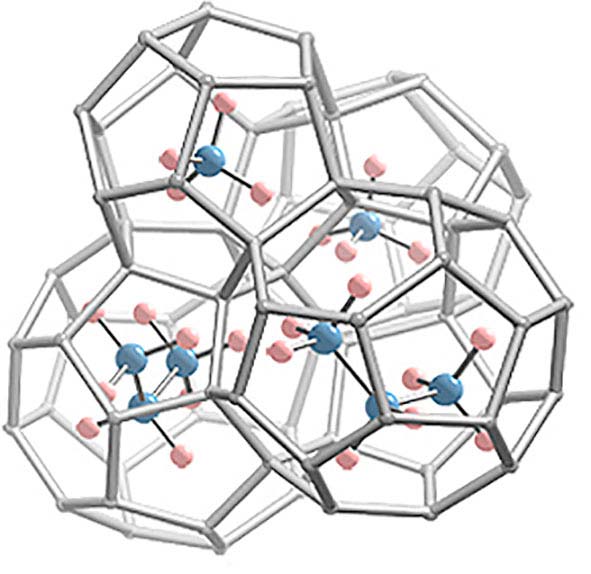
На схеме: кристаллическая структура гидрата метана, в вершинах многогранников расположены центры атомов кислорода, ребро является водородной связью (элементарная ячейка: 6Т×2D×46H2O).
|
620049, г. Екатеринбург, ул. Первомайская, 91 +7(343) 374-07-47 |